Les chéloïdes représentent une préoccupation médicale et esthétique majeure affectant des millions de personnes dans le monde. Ces cicatrices pathologiques, caractérisées par une prolifération excessive de tissu fibreux, peuvent survenir après diverses lésions cutanées, notamment les piercings, interventions chirurgicales ou traumatismes. Contrairement aux cicatrices normales, les chéloïdes débordent largement de la zone initialement lésée et persistent indéfiniment sans traitement approprié. La compréhension des mécanismes physiopathologiques et l’identification des facteurs de risque constituent les fondements d’une prise en charge thérapeutique optimale. L’arsenal thérapeutique moderne offre heureusement plusieurs approches prometteuses, depuis les injections de corticostéroïdes jusqu’aux techniques de pointe par laser fractionné.
Physiopathologie et classification des cicatrices chéloïdiennes selon rockwell
Mécanismes de surproduction collagénique dans le derme réticulaire
La formation d’une chéloïde résulte d’un dérèglement complexe du processus normal de cicatrisation au niveau du derme réticulaire. Les fibroblastes, cellules responsables de la synthèse du collagène, présentent une activité anormalement élevée et prolongée. Cette hyperactivité conduit à une surproduction massive de collagène de type I et III, créant des dépôts fibreux désorganisés qui s’accumulent progressivement dans les couches profondes de la peau.
Le processus inflammatoire chronique joue un rôle déterminant dans la perpétuation de cette anomalie cicatricielle. Les cytokines pro-inflammatoires, notamment le TGF-β (Transforming Growth Factor-beta), stimulent de manière excessive la prolifération fibroblastique. Cette cascade inflammatoire maintient un état d’hyperproduction collagénique qui peut persister durant des années, expliquant pourquoi les chéloïdes continuent de croître bien après la guérison initiale de la plaie.
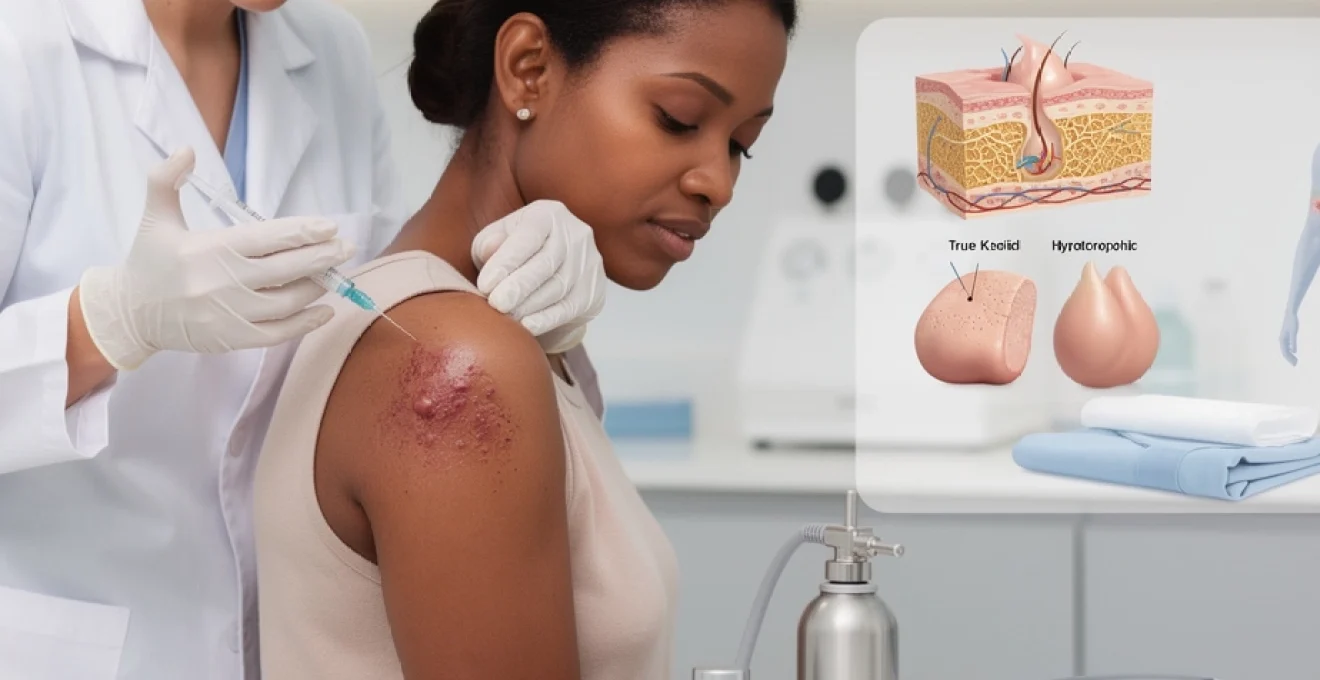
Différenciation entre chéloïdes vraies et cicatrices hypertrophiques
La distinction entre chéloïdes vraies et cicatrices hypertrophiques constitue un élément diagnostique fondamental. Les cicatrices hypertrophiques restent confinées dans les limites de la lésion initiale et montrent une tendance spontanée à l’amélioration après 12 à 18 mois. En revanche, les chéloïdes débordent systématiquement au-delà des bordures de la plaie originelle et ne présentent aucune régression spontanée.
La classification temporelle établit qu’une cicatrice épaisse persistant au-delà de 18 mois sans amélioration correspond définitivement à une chéloïde vraie.
Cette différenciation revêt une importance capitale pour orienter les choix thérapeutiques. Les cicatrices hypertrophiques répondent généralement mieux aux traitements conservateurs, tandis que les chéloïdes nécessitent souvent des approches plus agressives combinant plusieurs modalités thérapeutiques pour obtenir des résultats satisfaisants.
Facteurs génétiques et prédisposition ethnique aux chéloïdes
La susceptibilité aux chéloïdes présente une composante génétique marquée, avec des variations significatives selon l’origine ethnique. Les populations d’origine africaine et asiatique affichent une prévalence particulièrement élevée, pouvant atteindre 15 à 20% dans certaines régions. Cette prédisposition s’explique par des
variations dans la réponse inflammatoire, dans la structure du collagène et dans l’activité des fibroblastes. Plusieurs études familiales ont mis en évidence un caractère autosomique dominant à pénétrance variable, ce qui signifie que si un parent au premier degré présente des chéloïdes, le risque pour la descendance est nettement augmenté. Des polymorphismes de gènes impliqués dans la voie du TGF-β, de l’angiogenèse et de la synthèse de la matrice extracellulaire ont notamment été associés à cette cicatrisation excessive.
Au-delà de l’ethnie, d’autres facteurs génétiques et individuels entrent en jeu : âge jeune (en particulier entre 10 et 30 ans), antécédents personnels de cicatrices chéloïdiennes multiples, ainsi que certains terrains hormonaux. C’est la raison pour laquelle deux personnes exposées au même traumatisme cutané ne cicatriseront pas de la même façon. Pour vous comme pour votre médecin, identifier cette prédisposition permet d’anticiper les risques et d’adapter la stratégie de prévention et de traitement des chéloïdes dès la phase post-opératoire ou après un piercing.
Classification topographique des zones à haut risque chéloïdien
Toutes les zones cutanées ne sont pas égales face au risque de chéloïde. La classification topographique inspirée des travaux de Rockwell met en avant des régions « à haut risque » où les chéloïdes apparaissent plus fréquemment et avec un comportement plus agressif. Il s’agit principalement du sternum, des épaules, de la région scapulaire, de la nuque, du bas du visage (mandibule) et de la région pubienne. Les oreilles, notamment le lobe et le cartilage après piercing, font également partie des localisations classiques.
À l’inverse, certaines zones comme les paupières, les paumes, la plante des pieds ou le cuir chevelu sont très rarement le siège de chéloïdes. Cette répartition s’explique par des différences de tension cutanée, de densité en fibroblastes et d’exposition aux traumatismes répétés. Concrètement, si vous présentez un risque élevé (peau foncée, antécédents personnels), il est judicieux d’éviter les interventions esthétiques superflues dans ces zones à haut risque chéloïdien ou, au minimum, de prévoir des mesures préventives renforcées.
Protocoles thérapeutiques par injection de corticostéroïdes intralésionnels
Posologie optimale de triamcinolone acétonide selon la taille lésionnelle
Les injections intralésionnelles de corticostéroïdes constituent le traitement de première ligne des cicatrices chéloïdes de petite à moyenne taille. La molécule la plus utilisée est la triamcinolone acétonide (Kenacort), choisie pour sa puissance anti-inflammatoire et sa longue durée d’action locale. La posologie doit être adaptée au volume de la lésion pour être efficace sans majorer le risque d’atrophie cutanée.
En pratique, la concentration varie le plus souvent entre 10 et 40 mg/mL. Pour les petites chéloïdes (inférieures à 1 cm), des doses de 5 à 10 mg par séance suffisent généralement. Pour les lésions plus volumineuses, on peut aller jusqu’à 20–40 mg, en fractionnant l’injection sur toute la longueur de la cicatrice. L’objectif n’est pas de « remplir » la chéloïde de produit, mais d’obtenir une diffusion homogène du corticostéroïde dans l’ensemble du derme pathologique.
Techniques d’injection multiponctuelle et espacement thérapeutique
La technique d’injection joue un rôle aussi crucial que la dose. La plupart des spécialistes privilégient une approche multiponctuelle : à l’aide d’une aiguille fine (30G, voire 27G si la cicatrice est très fibreuse), le praticien réalise une série de petites injections espacées de quelques millimètres le long de la chéloïde. L’aiguille est introduite tangentiellement pour déposer le produit dans l’épaisseur du derme, là où la prolifération fibroblastique est maximale.
Les séances sont généralement espacées de 3 à 6 semaines, le temps d’évaluer la réponse clinique : diminution de l’épaisseur, assouplissement, disparition du prurit et des douleurs. Selon les séries, il faut souvent 3 à 6 séances pour obtenir un résultat significatif, parfois davantage pour des lésions anciennes. Vous vous demandez peut-être combien de temps ce traitement va durer ? Tout dépend du comportement de votre cicatrice, mais l’arrêt des injections est envisagé dès que la lésion est plate, souple et stable depuis plusieurs mois.
Gestion des effets secondaires : atrophie cutanée et télangiectasies
Comme tout traitement actif, les injections de corticostéroïdes intralésionnels comportent des effets secondaires potentiels. Les plus fréquents sont l’atrophie cutanée (amincissement de la peau) et l’apparition de télangiectasies (petits vaisseaux rouges en surface). Ils surviennent surtout lorsque les doses sont trop élevées ou les injections trop superficielles et trop rapprochées.
Pour limiter ces risques, le praticien veille à : utiliser la dose minimale efficace, injecter au cœur de la chéloïde et non dans la peau saine périphérique, et respecter un intervalle suffisant entre les séances. En cas d’atrophie localisée, il est recommandé de suspendre les injections sur cette zone et de prolonger l’intervalle thérapeutique. Dans la grande majorité des cas, ces anomalies esthétiques s’atténuent progressivement dans les mois qui suivent la fin du traitement.
Combinaison corticothérapie et cryothérapie à l’azote liquide
Pour les chéloïdes épaisses et résistantes, l’association de la corticothérapie intralésionnelle et de la cryothérapie à l’azote liquide offre souvent de meilleurs résultats qu’une monothérapie. La cryothérapie provoque une nécrose contrôlée du tissu fibreux par congélation, ce qui entraîne un amincissement de la cicatrice et améliore la pénétration ultérieure des corticostéroïdes.
Le protocole classique consiste à réaliser une ou plusieurs séances de cryothérapie (par pulvérisation ou sonde de contact) jusqu’à blanchiment de la lésion, puis, après quelques semaines de cicatrisation, à débuter ou reprendre les injections de triamcinolone. Cette stratégie « en deux temps » s’apparente à un travail de taille et de polissage : la cryothérapie réduit le volume, la corticothérapie stabilise et « éteint » l’activité chéloïdienne. Là encore, l’adaptation personnalisée est essentielle, car une cryothérapie trop agressive pourrait paradoxalement déclencher une nouvelle poussée chéloïde.
Thérapies ablatives par laser CO2 fractionné et radiofréquence
Les thérapies ablatives, en particulier le laser CO2 fractionné et certains dispositifs de radiofréquence, ont suscité un intérêt croissant dans la prise en charge des cicatrices complexes. Leur principe consiste à créer une multitude de microcolonnes de coagulation ou d’ablation dans la chéloïde, laissant entre chaque impact des ponts de peau saine qui facilitent la réparation. Cette micro-ablation permet de remodeler partiellement la matrice collagénique et d’améliorer la texture et la souplesse de la cicatrice.
Chez les patients à fort risque chéloïdien, ces techniques doivent toutefois être utilisées avec prudence. En effet, toute agression thermique de la peau peut potentiellement déclencher une nouvelle phase de cicatrisation anarchique. Les meilleures indications concernent les cicatrices mixtes hypertrophiques/chéloïdiennes stabilisées, en complément d’un traitement de fond (corticostéroïdes, silicone, compression). Dans ces cas, le laser CO2 fractionné ou la radiofréquence microaiguille peuvent améliorer le relief, la couleur et parfois les symptômes (démangeaisons, tiraillements), à condition de respecter des paramètres modérés et un espacement suffisant entre les séances.
Avant de recourir au laser pour « soigner un chéloïde efficacement », un bilan soigneux s’impose : type de peau (phototype), antécédents de mauvaises cicatrisations, localisation et ancienneté de la lésion. Dans de nombreuses situations, le laser ne sera pas le traitement de première intention, mais plutôt un outil de finition, intégré dans un protocole global après stabilisation de la chéloïde par des méthodes plus classiques. Vous l’aurez compris : mieux vaut éviter les promesses trop rapides de « gommage définitif » par laser, surtout si vous avez déjà fait des chéloïdes par le passé.
Approches chirurgicales et prévention des récidives post-opératoires
La chirurgie des chéloïdes est une arme à double tranchant. D’un côté, l’exérèse permet de réduire rapidement un volume cicatriciel très important, qui peut être douloureux, gênant fonctionnellement ou extrêmement inesthétique. De l’autre, toute incision cutanée chez un patient à risque de chéloïde expose à une récidive, parfois plus volumineuse que la lésion initiale si la technique n’est pas rigoureuse.
Le principe fondamental est celui de l’exérèse intra-cicatricielle : le chirurgien doit retirer la chéloïde en restant strictement à l’intérieur de la cicatrice, sans allonger la plaie ni empiéter sur la peau saine. L’objectif est de diminuer la masse fibreuse tout en limitant au maximum la surface d’agression cutanée. Dans certains cas extrêmes (énormes chéloïdes rétro-auriculaires ou sternales), une résection partielle en plusieurs temps peut être envisagée pour réduire progressivement le volume sans provoquer de tension excessive sur les berges.
La clé du succès réside ensuite dans la prévention de la récidive post-opératoire. Dès que la cicatrice est suffisamment consolidée (en général 3 à 4 semaines après l’exérèse), on met en place un protocole combinant plaques de silicone, compression locale (clips d’oreille, pansements compressifs ou vêtements sur-mesure) et injections intralésionnelles de triamcinolone si la moindre surépaisseur inflammatoire réapparaît. Dans les formes très rebelles, une curiethérapie (radiothérapie locale à faible dose) peut être discutée dans les jours suivant l’intervention, en centre spécialisé.
En pratique, se faire opérer d’une chéloïde ne doit jamais être une décision prise à la légère. Il s’agit d’un véritable « pari thérapeutique » qui doit être soigneusement pesé avec votre chirurgien plasticien, en tenant compte de votre âge, de la localisation, de la taille de la lésion et de votre vécu psychologique. Lorsque l’indication est bien posée et que la prévention est rigoureuse, la chirurgie peut néanmoins transformer de façon très positive l’aspect et le confort d’une cicatrice chéloïde majeure.
Traitements adjuvants : plaques de gel de silicone et compression thérapeutique
Efficacité des plaques Cica-Care et dermatix dans la réduction volumétrique
Les plaques de gel de silicone constituent l’un des piliers du traitement non invasif des cicatrices hypertrophiques et chéloïdes. Des produits comme Cica-Care ou Dermatix ont été largement étudiés et leur efficacité est aujourd’hui bien documentée dans la réduction de l’épaisseur, de la rougeur et de la rigidité cicatricielle. Leur action repose à la fois sur l’hydratation prolongée de la couche cornée, la normalisation de la température locale et une légère pression répartie sur la zone.
Pour obtenir un effet significatif, ces dispositifs doivent être portés de manière quasi continue, idéalement 12 à 24 heures par jour, pendant plusieurs mois. C’est souvent là que réside la difficulté : la constance. Vous vous demandez peut-être si ces plaques suffiront à « faire disparaître » une chéloïde ancienne et volumineuse ? Dans ce cas précis, elles auront surtout un rôle d’adjuvant, mais sur des lésions plus récentes ou de taille modérée, elles peuvent à elles seules permettre un aplanissement progressif très satisfaisant, en particulier si elles sont introduites précocement après la fermeture de la plaie.
Protocoles de compression continue et vêtements compressifs sur-mesure
La compression thérapeutique, ou pressothérapie, est une autre arme efficace pour contrôler l’évolution des chéloïdes. Le principe est simple : exercer une pression continue et homogène sur la cicatrice pour « asphyxier » partiellement les fibroblastes hyperactifs, réduire l’apport sanguin local et limiter la synthèse de collagène. Cela se traduit au fil des mois par une cicatrice plus plane, plus souple et moins rouge.
Selon la localisation, différents dispositifs sont utilisés : clips d’oreille après chirurgie de chéloïde auriculaire, pansements compressifs siliconés pour le thorax ou l’épaule, ou encore vêtements compressifs sur-mesure (gilets, boléros, manchons) pour les lésions étendues, notamment après brûlure. Les protocoles recommandent souvent un port de 23 heures sur 24 pendant au moins 6 mois, parfois jusqu’à 12 mois dans les formes sévères. Autant dire que votre motivation et votre confort (choix des matières, ajustement correct) seront déterminants pour tenir dans la durée.
Surveillance dermatoscopique de l’évolution lésionnelle
Quel que soit le traitement choisi pour soigner un chéloïde efficacement, la surveillance régulière de son évolution est essentielle. Au-delà de l’examen clinique classique (palpation, mesure de l’épaisseur, appréciation de la couleur et de la souplesse), certains praticiens utilisent la dermatoscopie pour analyser plus finement la vascularisation, la texture de surface et d’éventuelles zones de récidive précoce. Cet outil non invasif permet d’objectiver les progrès ou, au contraire, de détecter rapidement une reprise évolutive.
Concrètement, des consultations espacées de 1 à 3 mois sont organisées pendant la phase active du traitement, puis tous les 6 à 12 mois une fois la cicatrice stabilisée. C’est l’occasion de réajuster votre protocole : poursuivre ou interrompre les plaques de silicone, diminuer la pression d’un vêtement compressif, espacer les injections de corticostéroïdes, ou encore renoncer à un geste laser si la lésion paraît trop instable. Cette approche dynamique et personnalisée est la meilleure garantie d’un résultat durable, tant sur le plan esthétique que fonctionnel.